HƯỚNG DẪN SỬ DỤNG
Tên thuốc: HADUFOVIR
Đọc kỹ hướng dẫn sử dụng trước khi dùng. Để xa tầm tay trẻ em.
Thuốc này chỉ dùng theo đơn thuốc
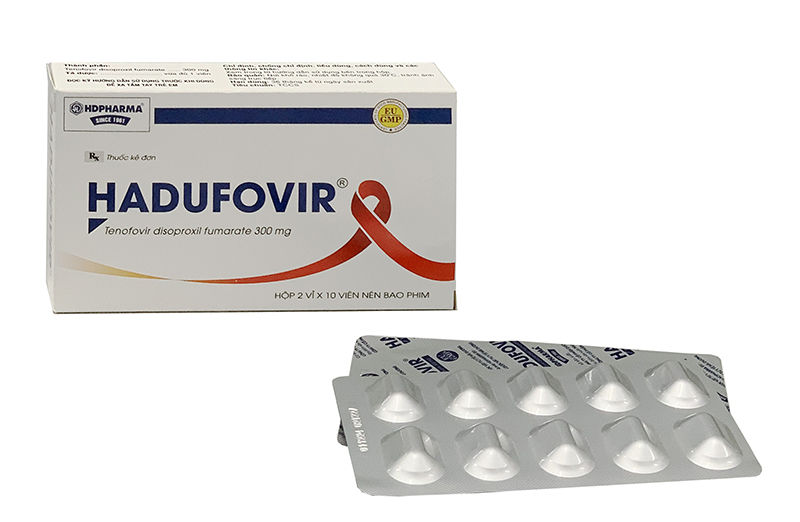
1. Thành phần công thức thuốc:
Thành phần hoạt chất:
Tenofovir disoproxil fumarate …..300 mg
Thành phần tá dược: Lactose monohydrate đã nghiền, Maize starch B, Microcrystalline Cellulose, Polyvinyl pyrolidon K30, Magnesi stearat, Sodium croscarmelose, Hydroxypropyl methylcellulose 606, Hydroxypropyl methylcellulose 615, Polyethylene glycol 6000, Talc, Titan dioxyd, màu Briliant Blue…..Vừa đủ 1 viên
2. Dạng bào chế: Viên nén bao phim, hình thuôn dài, bề mặt nhẵn, bóng, màu xanh, bên trong màu trắng.
3. Chỉ định
Viên nén bao phim Hadufovir 300 mg chứa hoạt chất là tenofovir disoprosil fumarat, đây là một chất kháng virus, được sử dụng để điều trị nhiễm HIV, HBV hoặc nhiễm cả 2 virus này.
– Kết hợp với các thuốc kháng retrovirus khác để điều trị nhiễm HIV-1, điều trị viêm gan B mạn tính ở người lớn và thanh thiếu niên từ 12 đến dưới 18 tuổi với cân nặng thấp nhất là 35 kg.
– Kết hợp với thuốc kháng retrovirus khác trong dự phòng cho các cán bộ y tế phải tiếp xúc với các bệnh phẩm (máu, dịch cơ thể…) có nguy cơ lây nhiễm HIV. 4. Cách dùng, liều dùng:
4.1. Liều dùng – Cách dùng:
Liều dùng của thuốc được khuyến nghị ở bệnh nhân trên 12 tuổi và cân nặng ít nhất 35 kg, cụ thể:
+ Điều trị nhiễm HIV – 1: uống 1 viên 300 mg, 1 lần mỗi ngày, uống đúng giờ.
+ Điều trị viêm gan B mãn tính: Uống 1 viên/lần/ngày. Thời gian ngừng thuốc tối ưu chưa biết. Có thể ngừng:
Ở người bệnh có AgHBe (+), không xơ gan: Điều trị ít nhất 6 – 12 tháng sau khi xác định có huyết thanh chuyển đổi HBe (AgHBe (-), không phát hiện được ADN của virus viêm gan B và có kháng -HBe) hoặc tới khi có huyết thanh chuyển đổi HBs hoặc khi thấy thuốc mất tác dụng. Tỷ lệ ALT huyết thanh và ADN của virus viêm gan B phải được kiểm tra đều đặn sau khi ngừng điều trị để phát hiện bất cứ một tái phát nào muộn. Ở người bệnh có AgHBe (-), không xơ gan: Điều trị phải kéo dài cho tới khi huyết thanh chuyển đổi HBs hoặc cho tới khi thấy thuốc không còn tác dụng. Trong trường hợp điều trị kéo dài trên 2 năm nên được đánh giá lại đều đặn để xác định xem theo đuổi điều trị như vậy có phù hợp với người bệnh không. Nếu ngừng tenofovir disoproxil fumarat ở người bệnh bị viêm gan man tính đồng thời có nhiễm HIV, phải theo dõi người bệnh chặt chẽ để phát hiện tất cả những dấu hiệu nặng lên của viêm gan. Điều trị phải do thầy thuốc có kinh nghiệm. Nên làm một test phát hiện kháng thể kháng HIV cho các người bệnh bị nhiễm virus viêm gan B trước khi bắt đầu điều trị bằng tenofovir disoproxil fumarat.
+ Dự phòng nhiễm HIV do phơi nhiễm với HIV – 1: Phải dùng kết hợp với các thuốc kháng retrovirus khác. Phải dùng thật sớm, trong vòng vài giờ sau khi phơi nhiễm. Uống 1 viên 300 mg/lần/ngày và trong 4 tuần nếu được dung nạp tốt.
Thuốc chưa được nghiên cứu cho trẻ em dưới 18 tuổi và người cao tuổi trên 65 tuổi.
– Liều dùng cho đối tượng đặc biệt:
Liều khuyến cáo ở bệnh nhân trưởng thành bị suy giảm chức năng thận:
+ Bệnh nhân có độ thanh thải creatinin (CrCI) trong khoảng: 30–49 ml/ phút: uống 1 viên 300 mg mỗi lần , 2 ngày uống 1 lần.
+ CrCl trong khoảng 10–29 ml/ phút: uống 1 viên 300 mg mỗi lần , 3-4 ngày uống 1 lần.
+ Chạy thận nhân tạo: uống 1 viên 300 mg một lần mỗi tuần hoặc sau khi lọc máu khoảng 12 giờ.
Liều dùng cho đối tượng suy gan: Không cần hiệu chỉnh liều cho đối tượng bệnh nhân suy gan.
Nếu ngừng dùng tenofovir ở bệnh nhân viêm gan B mãn tính có hoặc không đồng nhiễm HIV, những bệnh nhân này cần được theo dõi chặt chẽ để tìm bằng chứng về đợt cấp của
viêm gan (xem phần 6).
4.2. Cách dùng:
Dùng thuốc theo đường uống.
Thời điểm uống thuốc: Thường được uống 1 lần trong ngày, uống đúng giờ và nên uống thuốc kèm với thức ăn. Uống ngay liều thuốc đã quên càng sớm càng tốt. Tuy nhiên, nếu đã quên quá 12 giờ và gần đến giờ uống liều tiếp theo thì giữ nguyên, không nên uống dồn 2 liều thuốc liền nhau.
5. Chống chỉ định:
Bệnh nhân quá mẫn cảm với tenofovir hoặc với bất kỳ thành phần nào của thuốc. Phụ nữ có thai và cho con bú.
6. Quá liều và cách xử trí:
6.1. Quá liều:
Triệu chứng: Chưa có số liệu đầy đủ về quá liều. Nếu có nghi ngờ quá liều xảy ra, bệnh nhân phải được theo dõi bằng chứng về độc tính.
6.2. Xử trí:
Tenofovir có thể được loại bỏ bằng thẩm tách máu; độ thanh thải thẩm tách trung bình của tenofovir là 134 ml / phút, có thể thẩm phân màng bụng để làm tăng tốc độ đào thải tenofovir. Tuy nhiên, chưa rõ phương pháp này có làm thay đổi bệnh cảnh lâm sàng của quá liều thuốc hay không.
7. Điều kiện bảo quản, hạn dùng, tiêu chuẩn chất lượng của thuốc:
– Điều kiện bảo quản: Để nơi khô ráo, nhiệt độ không quá 30°C, tránh ánh sáng trực tiếp.
– Hạn dùng: 36 tháng kể từ ngày sản xuất.
– Tiêu chuẩn chất lượng: TCCS.
Tên, địa chỉ của cơ sở sản xuất thuốc:
CÔNG TY CỔ PHẦN DƯỢC VẬT TƯ Y TẾ HẢI DƯƠNG
NHÀ MÁY HDPHARMA EU – CÔNG TY CỔ PHẦN DƯỢC VẬT TƯ Y TẾ HẢI DƯƠNG
Tầng 2, tòa nhà 4A, thửa đất số 307 cụm công nghiệp Cẩm Thượng, phường Cẩm Thượng, TP. Hải Dương, Tỉnh Hải Dương
Tel: 0220.3853.848
Lưu ý: Những thông tin trên dành cho nhân viên y tế và mang tính chất trợ giúp tìm hiểu về sản phẩm, không nhằm mục đích quảng cáo.
HDPHARMA

 LIÊN HỆ
LIÊN HỆ VN
VN EN
EN


Reviews
There are no reviews yet.